Kalium nitrat (KNO3) - qeyri -üzvi bir birləşmədir, nitrat turşusunun kalium duzuna deyilir.
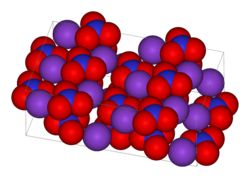
| Kalium nitrat | |
|---|---|
 | |
 | |
| Ümumi | |
| Sistematik adı | Kalium nitrat |
| Kimyəvi formulu | KNO3 |
| Fiziki xassələri | |
| Molyar kütlə | 101,1032 q/mol |
| Sıxlıq | 2,109 (16 °C) q/sm³ |
| Bərklik | 2 |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 334 °C |
| Qaynama nöqtəsi | 400 °C |
| Əmələgəlmə entalpiyası | −494 kC/mol |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 7757-79-1 |
| PubChem | 24434, 139063997, 516903 |
| EINECS-də qeyd. nöm. | 231-818-8 |
| SMILES | |
| InChI | |
| E nömrəsi | E252 |
| RTECS | TT3700000 |
| ChEBI | 63043 |
| BMT nömrəsi | 1486 |
| ChemSpider | 22843 |
| Məlumatlar normal şərait (25 °C, 100 kPa) üçün verilmişdir. | |
Təbiətdə tapılması
Təbiətdə nitrokalit mineralı kimi tanınır. Təbii kalium nitrat azot tərkibli maddələrin parçalanması nəticəsində tapılır. Bitkilərdə və heyvanlarda çox az miqdarda olur.
Fiziki xassələri
Alınması
Gübrənin çürüməsi nəticəsində azot əmələ gəlir və saman qatlarında toplanaraq nitrifikasiyaya məruz qalır və əvvəlcə azotlu, sonra isə nitrat turşusuna çevrilir. Nitrat turşusu əhəngdaşı ilə qarşılıqlı təsir göstərərək, su ilə yuyulmuş Ca(NO3)2 alınırdı. Odun külünün əlavə edilməsi CaCO3 çökdürdü və kalium nitrat məhlulu əmələ gətirdi. Çox zaman əhəng daşı əvəzinə yığına dərhal kül əlavə edilir və kalium nitrat alınır.
1854-cü ildə alman kimyaçısı K. Nöllner daha əlverişli və daha ucuz kalium xlorid və natrium nitratın reaksiyasına əsaslananaraq kalium nitrat istehsal etdi:
Kalium nitratın alınmasının bir neçə başqa yoluda var. Bu, ammonium nitratın kalium xlorid ilə reaksiyası nəticəsində baş verir, kalium nitrat və ammonium xlorid alınır, sonuncu asanlıqla ayrılır:
Kalium hidroksidin və ya kalium karbonatın reaksiyası nəticəsində:
Kimyəvi xassələri
400-520 °C temperaturda parçalanır və nəticədə kalium nitrit KNO2 və oksigen O2 alınır (oksigenin ayrılması kalium nitratın yanğın təhlükəsini artırır):
Güclü osidləşdiricidir. Kalium nitratın qarışıqları üzvi maddələrlə birləşəndə partlayış baş verə bilər. Ayrılma zamanı hidrogenlə reduksiya olunur ( duru xlorid turşusudur):
Kalium nitratın əriməsi ilə kalium metalını elektroliz yolu ilə əldə etmək olar, lakin kalium nitratın yüksək oksidləşdirici qabiliyyətinə görə kalium hidroksidinə üstünlük verilir.
Tətbiqi
Kalium nitratın əsas tətbiqi, qiymətli bir gübrə olaraq qalmasıdır. Elektrovakuum sənayesində və optik şüşəqayırmada texniki şüşələrin rəngini dəyişmək və aydınlaşdırmaq və şüşə məmulatlarına möhkəmlik vermək üçün istifadə olunur. Metallurgiyada, xüsusən nikel filizlərinin emalında güclü oksidləşdirici vasitə kimi istifadə olunur. Qida sənayesində kalium nitrat E 252 konservantı kimi istifadə olunur.
vikipedia, viki, ensiklopediya, kitab, məqalə, oxumaq, pulsuz yüklə, Kalium nitrat haqqında məlumat. Kalium nitrat nədir? Kalium nitrat nə deməkdir?
 Azərbaycanca (AZ)
Azərbaycanca (AZ) English (US)
English (US) Қазақша (KZ)
Қазақша (KZ) Lietuva (LT)
Lietuva (LT) Türkçe (TR)
Türkçe (TR) O'zbekcha (UZ)
O'zbekcha (UZ)








