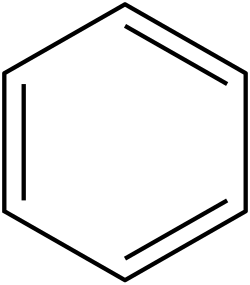
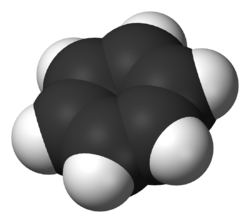
Benzol (C6H6) — üzvi maddələr sinfinə daxil olan özünəməxsus, xoş, şirintəhər iyə malik, şəffaf maye. Benzol bəzən Benzen adı ilə də səslənir.
| Benzol | |
|---|---|
 | |
 | |
| Ümumi | |
| Kimyəvi formulu | C6H6 |
| Fiziki xassələri | |
| Molyar kütlə | 78,11 q/mol |
| Sıxlıq | 0,8786 q/sm³ |
| Dinamik özüllülük | 0,0652 puazeyl |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 5,5 °C |
| Qaynama nöqtəsi | 80,1 °C |
| Öz-özünə yanma temperaturu | 498 ± 1 °C |
| Partlama həddi | 1,2 ± 0,1 % (V/V) |
| Əmələgəlmə entalpiyası | 82.930 C/mol, 49.080 C/mol |
| Buxarın təzyiqi | 75 ± 1 mm Hg |
| Optik xüsusiyyətlər | |
| Sındırma əmsalı | 1,501 |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 71-43-2 |
| PubChem | 241 |
| EINECS-də qeyd. nöm. | 200-753-7 |
| SMILES | |
| InChI | |
| RTECS | CY1400000 |
| ChEBI | 16716 |
| BMT nömrəsi | 1114 |
| ChemSpider | 236 |
| Məlumatlar normal şərait (25 °C, 100 kPa) üçün verilmişdir. | |
Tarix

1865-ci ildə Alman alimi Fridrix Avqust Kekule (Bonn Universitetini bitirmişdir) benzola tsikloheksatrien (C6H6) kimi quruluş vermişdir. Sonralar benzol üçün daha bir sıra quruluşlar təklif olunmuşdur. Kekule formulundan bu günə kimi istifadə olunmasına baxmayaraq, o, benzolun xassələrini tam əks etdirmir. Belə ki, Kekule formulu benzolun birləşmə reaksiyasına daxil olmasını izah etdiyi halda, benzol üçün birləşmə reaksiyasının deyil, əvəzlənmə reaksiyasının xarakter olması, onun termodinamik və oksidləşdiricilərə qarşı davamlığı izah olunmamış qahrdı. Digər tərəfdən Kekule formuluna görə benzolun izomerdən 1,2-diəvəzli törəmələri ikidən ibarət olmalıdır. Lakin belə izomerlərin olması heç vaxt müşahidə olunmamışdır. Kekule bunu düzgün olaraq benzolda ikiqat əlaqələrin osillasiyası (yerlərini dəyişməsi) ilə izah edirdi.
Hazırda müxtəlif üsullarla təsdiq edilmişdir ki, benzol molekulu koplanardır,yəni benzolda bütün atomlar bir müstəvi üzərində yerləşir və karbon atomlarındakı qoşulmuş π-elektron orbitalları həmin müstəviyə perpendikulyardır.
Maraqlı faktlar
- Əfsanəyə görə, Kekule Benzolun formulunu 1862-ci ildə yuxuda görmüşdür. O, yuxuda öz quyruğunu dişləyən ilan gördükdən sonra formulu fikirləşmişdir.
Kimyəvi xassələri
Benzol üçün xarakterik reaksiyalar:
- Alkenlərlə qarşılıqlı təsiri nəticəsində etilbenzol və kumol alınır:
- xlorbenzol əmələ gətirmək üçün katalizatorun iştirakı ilə xlor və brom ilə qarşılıqlı təsir ( elektrofil əvəzetmə reaksiyası):
- Katalizator olmadıqda qızdırılma və ya işıqlandırma zamanı heksaxlorosikloheksan izomerlərinin qarışığının əmələ gəlməsi
- Oleum məhlulunda benzol bromla reaksiyaya girdikdə heksabromobenzol əmələ gəlir:
- Alkanların halogen törəmələri ilə alkilbenzolların əmələ gəlməsi ilə qarşılıqlı əlaqə (benzol alkilləşməsi, Friedel-Krafts reaksiyası):
- Friedel-Crafts asilləşmə reaksiyası
- Formilləşmə reaksiyası, benzolun CO və HCl qarışığı ilə qarşılıqlı təsiridir, yüksək təzyiqdə və katalizatorun təsiri altında davam edir, reaksiya məhsulu benzaldehiddir:
- Sulfonlaşma və nitrollaşma reaksiyaları (elektrofil əvəzetmə):
- Benzolun hidrogenlə azaldılması (katalitik hidrogenləşmə):
Benzolun oksidləşməsi
Benzol, strukturuna görə, oksidləşməyə çox davamlıdır
- Ozonolaşma reaksiyası.
Reaksiya nəticəsində dialdehid - qlioksal (1,2-etandial) əmələ gəlir.
- Yanma reaksiyası. Benzolun yanması oksidləşmənin məhdudlaşdırıcı halıdır. Benzol çox alovlanır və havada yüksək dumanlı alovla yanır (hər molekulda 92%-ə qədər karbon var):
Ədəbiyyat
- Энциклопедический словарь юного химика / Сост. В. А. Крицман, В. В. Станцо. — М.: Педагогика, 1982. — 368 с., ил.
- Настольная книга учителя химии 10 класс/О. С. Габриелян, И. Г. Остроумов. — М.:Дрофа, 2004 г.
Həmçinin bax
vikipedia, viki, ensiklopediya, kitab, məqalə, oxumaq, pulsuz yüklə, Benzol haqqında məlumat. Benzol nədir? Benzol nə deməkdir?
 Azərbaycanca (AZ)
Azərbaycanca (AZ) English (US)
English (US) Қазақша (KZ)
Қазақша (KZ) Lietuva (LT)
Lietuva (LT) Türkçe (TR)
Türkçe (TR) O'zbekcha (UZ)
O'zbekcha (UZ)
![{\displaystyle {\mathsf {C_{6}H_{6}+H_{2}C=CH_{2}{\xrightarrow[{}]{AlCl_{3}*HCl}}C_{6}H_{5}CH_{2}CH_{3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c3f61f139eb31a72d2326c147249a7b908c2ac6a)
![{\displaystyle {\mathsf {C_{6}H_{6}+CH_{2}=CH-CH_{3}{\xrightarrow[{}]{AlCl_{3}*HCl}}C_{6}H_{5}CH(CH_{3})_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4f081cd141db22599728e1b240c5ec7ab6baa565)
![{\displaystyle {\mathsf {C_{6}H_{6}+Cl_{2}{\xrightarrow[{}]{FeCl_{3}}}C_{6}H_{5}Cl+HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d48ae47e593005848b4abfd855049b67f6f5ea50)
![{\displaystyle {\mathsf {C_{6}H_{6}+3Cl_{2}{\xrightarrow[{}]{T,h\nu }}C_{6}H_{6}Cl_{6}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b9d2fca06a46bc66d3ec45fca4c8b05fadc9ba77)
![{\displaystyle {\mathsf {C_{6}H_{6}+6Br_{2}{\xrightarrow[{}]{H_{2}SO_{4}*SO_{3}}}C_{6}Br_{6}+6HBr}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aa58709f8d9ac9ddc486511a31790493ba04ac76)
![{\displaystyle {\mathsf {C_{6}H_{6}+(CH_{3}CO)_{2}O{\xrightarrow[{}]{AlCl_{3}}}C_{6}H_{5}COCH_{3}+CH_{3}COOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5ec9b3daf42ffc4dcae8dbab7396c44b330c1aa5)
![{\displaystyle {\mathsf {C_{6}H_{6}+C_{6}H_{5}COCl{\xrightarrow[{}]{AlCl_{3}}}C_{6}H_{5}COC_{6}H_{5}+HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2182024b1f4e61dfb52a2ef863d78d62105fb28a)
![{\displaystyle {\mathsf {C_{6}H_{6}+CO+HCl{\xrightarrow[{}]{AlCl_{3}}}C_{6}H_{5}COH+HCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1782d8565b8315504f780c576b6f91502454da79)
![{\displaystyle {\mathsf {C_{6}H_{6}+HNO_{3}{\xrightarrow[{}]{H_{2}SO_{4}}}C_{6}H_{5}NO_{2}+H_{2}O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ce592053321be27ccfa295dc0a41142fe6d5b4f6)

![{\displaystyle {\mathsf {C_{6}H_{6}+3H_{2}{\xrightarrow[{}]{Ni/Pd,Pt;t}}C_{6}H_{12}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/75c5a8c023361508ed63180efe6ded5d48b3acc7)
