Xlorid turşusu (HCl) — hidrogen və xlor elementlərindən ibarət olan, otaq istiliyi və normal təzyiqdə qaz halında olan kimyəvi bir mürəkkəbdir. IX əsrdə ərəb kimyaçı Cabir min Həyyan tərəfindən kəşf edildi və sonra simə sahəsində istifadə edildi. Sənaye İnqilabı əsnasında sənayedəki əhəmiyyəti kəşf edilən turşu əvvəl Leblanc əməliyyatı, sonra Solvay əməliyyatı ilə sənaye sahəsində istehsal olunmağa başladı. Xlorid turşusu tarixdə yeni asanlıqların kəşfində əhəmiyyətli rollar oynadı. Hal-hazırda PVC'den dəmir-polada, orqanik maddə istehsalından qida sektoruna qədər az qala bütün sahələrdə xlorid turşusundan istifadə edilməkdədir.
| Xlorid turşusu | |
|---|---|
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | −30 °C, −114,18 °C |
| Qaynama nöqtəsi | −85 °C |
| Buxarın təzyiqi | 190 hPa |
| Kimyəvi xassələri | |
| Turşunun dissosasiya sabiti | −6,3 ± 0,1 |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 7647-01-0 |
| EINECS-də qeyd. nöm. | 933-977-5 |
| E nömrəsi | E507 |
| RTECS | MW4025000 |
| Məlumatlar normal şərait (25 °C, 100 kPa) üçün verilmişdir. | |
Xlorid turşusu, təmin etdiyi asanlıqlara baxmayaraq, zəhərli bir maddədir və insan toxumaları başda olmaq üzrə çoxu səthə böyük təxribat verir. Bu səbəblə bu turşu ilə çalışılarkən təhlükəsizlik tədbirləri ən üst səviyyədə tutulmalıdır. Turşu, toksik olmasıyla bərabər, gözlər və dəri üçün tahriş edəndir, dəridə yanıqlara səbəb olmaqdadır və tənəffüs sistemi üçün tahriş edici xüsusiyyət daşımaqdadır. Hidrogen xlor, normal şərtlərdə −27.32 °C də əriyər, 110 °C də qaynar. Xlorid turşusu əldə edə bilmək üçün əvvəlcə hidrogen xlor gazınının əldə etmək lazımdır. QEYD- HCl- un Ca duzu su ilə kristalhidrat əmələ gətirir (CaCl•4HOH)
Fiziki xassələri
Cədvəldə müxtəlix konsentrasiyalı Xlorid turşusunun fiziki xassələri göstərilmişdir:
| Kons. (çəki) s : kq HCl/kq | Kons. (q/l) s : kq HCl/m³ | Sıxlıq ρ : kq/l | Molyarlıq M | pH | Özlülük η : mPa·s | Xüsusi istilik tutumu s : kC/(kq·К) | Buxarların təzyiqi PHCl : Pa | Т qaynama t.qay. | Т ərimə t.ər. |
| 10 % | 104,80 | 1,048 | 2,87 M | −0,5 | 1,16 | 3,47 | 0,527 | 103 °C | −18 °C |
| 20 % | 219,60 | 1,098 | 6,02 M | −0,8 | 1,37 | 2,99 | 27,3 | 108 °C | −59 °C |
| 30 % | 344,70 | 1,149 | 9,45 M | −1,0 | 1,70 | 2,60 | 1,410 | 90 °C | −52 °C |
| 32 % | 370,88 | 1,159 | 10,17 M | −1,0 | 1,80 | 2,55 | 3,130 | 84 °C | −43 °C |
| 34 % | 397,46 | 1,169 | 10,90 M | −1,0 | 1,90 | 2,50 | 6,733 | 71 °C | −36 °C |
| 36 % | 424,44 | 1,179 | 11,64 M | −1,1 | 1,99 | 2,46 | 14,100 | 61 °C | −30 °C |
| 38 % | 451,82 | 1,189 | 12,39 M | −1,1 | 2,10 | 2,43 | 28,000 | 48 °C | −26 °C |
Bərkimə zamanı HCl·H2O, HCl·2H2O, HCl·3H2O, HCl·6H2O tərkibli kristalhidratlar əmələ gətirir. 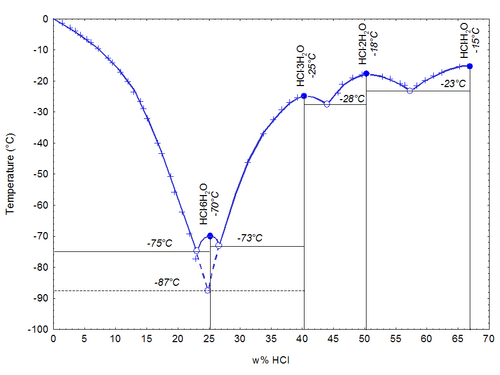
Kimyəvi xassələri
- Metalların elektromənfilik cədvəlində hidrogenə qədər olan metallarla qarşılıqlı təsirdə olub müvafiq duz və hidrogen əmələ gəlir:
- Metalların oksidləri ilə qarşılıqlı əlaqədə olub duz və su əmələ gətirir:
- Metalların hidroksidləri ilə neytrallaşma reaksiyasına daxil olub duz və su əmələ gətirir:
- Daha zəif turşuların duzları ilə qarşılıqlı təsiri:
- Güclü oksidləşdiricilərlə qarşılıqlı təsiri:
Tətbiqi
Xlorid turşusunun duzları geniş tətbiqə malikdir:
Daş və ya xörək duzu NaCl - xlorun, natrium-hidroksidin, metallik natriumun, hidrogen-xloridin və sodanın alınmasında xammal kimi geniş tətbiq olunur.
Kalium-xlorid KCl- kalium gübrəsi kimi, eləcə də potaş və digər kalium duzlarının alınmasında xammal kimi tətbiq olunur.
Gümüş xlorid AgCl - fotoqrafiyada tətbiq olunur.
Alüminium xlorid AlCl3 - üzvi sintezlərdə katalizator kimi istifadə edilir.
Barium xlorid BaCl2 - kənd təsərrüfatında kimyəvi zəhər kimi tətbiq olunur.
vikipedia, viki, ensiklopediya, kitab, məqalə, oxumaq, pulsuz yüklə, Xlorid turşusu haqqında məlumat. Xlorid turşusu nədir? Xlorid turşusu nə deməkdir?
 Azərbaycanca (AZ)
Azərbaycanca (AZ) English (US)
English (US) Қазақша (KZ)
Қазақша (KZ) Lietuva (LT)
Lietuva (LT) Türkçe (TR)
Türkçe (TR) O'zbekcha (UZ)
O'zbekcha (UZ)











