Tetraflüoretilen - C2F4 kimyəvi formulu olan karbon və flüorun üzvi birləşməsidir, flüorolefinlərin nümayəndələrindən biridir - doymamış flüor üzvi birləşmələrin.
| Tetraflüoretilen | |
|---|---|
 | |
 | |
| Ümumi | |
| Sistematik adı | Tetraflüoretilen |
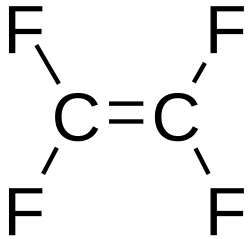
| Kimyəvi formulu | C2F4 |
| Fiziki xassələri | |
| Molyar kütlə | 100,016 q/mol |
| Sıxlıq | 1,43; 1,50138(0°C), 1,4555 q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | −131,15 °C |
| Qaynama nöqtəsi | −76,5 °C |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 116-14-3 |
| PubChem | 8301 |
| EINECS-də qeyd. nöm. | 204-126-9 |
| SMILES | |
| InChI | |
| ChEBI | 38866 |
| ChemSpider | 8000 |
| Məlumatlar normal şərait (25 °C, 100 kPa) üçün verilmişdir. | |
Fiziki xassələri
Tetraflüoretilen ağır qazdır (havadan demək olar ki, 3,5 dəfə ağırdır), rəngsiz və qoxusuzdur. Tetraflüoretilen molekulu düzdür, C–C nüvələrarası məsafə 1,33±0,06 Å, C–F nüvələrarası məsafə 1,30±0,02 Å, F–C–F bucaq arası rabitə 114±3°-dir.
Alınması
Laboratoriya şəraitində 1,2-dibromtetraflüoretanı sinklə debromlaşma reaksiyasına uğradaraq tetraflüoretileni almaq olar:
- ,
və ya texniki vakuumda politetraflüoretileni depolimerləşdirərək:
- .
Tetraflüoretilen sənayedə diflüorxlorometandan (freon-22) alınır. Proses iki mərhələdən ibarətdir:
- .
- ,
- .
Birinci mərhələdə xloroformu susuz hidrogen flüoridlə flüorlaşdırırıq. Bu proses avtoklavda təxminən 100°C temperaturda və 3 MPa təzyiqdə azot oksidinin iştirakı ilə aparılır. Monodiflüorxlormetanın çıxımı 80% təşkil edir. İkinci mərhələdə tetraflüoretileni diflüorxlorometa- nın (freon-22) pirolizi nəticəsində alırıq. Diflüorxlormetanın pirolizi gümüş boru şəklində olan reaktorda 600-800°C temperaturda aparılır. Tetraflüoretilenin çıxımı 90%-dən çox təşkil edir. Təmiz tetraflüoretilen otaq temperaturundan aşağı temperaturda polimerləşir. Buna görə də, o polimerləşmə inhibitorı olan - butilmerkaptanın (0,5%) iştirakı ilə saxlanılır.
Kimyəvi xassələri
Palladium katalizatorunda tetraflüoretilen hidrogenlə birləşir və 1,1,2,2-tetraflüoretan alınır:
- .
Ağır şəraitdə tetraflüoretilen oksigendə yanaraq tetraflüormetan və karbon qazı alınır:
- .
Yüksək temperaturda tetraflüoretilen tsiklodimerləşmə reaksiyasına uğrayaraq oktaflüortsiklobutan alınır:
- .
Tetraflüoretilenin pirolizi heksaflüorpropilenin alınması ilə müşayiət olunur:
- .
Tətbiqi
Tetraflüoretilen əsasən teflonun istehsalında istifadə olunur.
Toksikliyi
Tetraflüoretilen zəhərli maddədir. Gözün və tənəffüs orqanlarının selikli qişasını qıcıqlandırır, yüksək konsentrasiyalarda mərkəzi sinir sisteminə mənfi təsir göstərir, ağciyərdə iltihaba səbəb olur. Ölümcül doza 200-955 mg/kg-dır.
vikipedia, viki, ensiklopediya, kitab, məqalə, oxumaq, pulsuz yüklə, tetraflüoretilen sözünün mənası, tetraflüoretilen haqqında məlumat. tetraflüoretilen nədir? tetraflüoretilen nə deməkdir?
 Azərbaycanca (AZ)
Azərbaycanca (AZ) Deutsch (DE)
Deutsch (DE) English (US)
English (US) Қазақша (KZ)
Қазақша (KZ) Lietuva (LT)
Lietuva (LT) සිංහල (LK)
සිංහල (LK) Türkçe (TR)
Türkçe (TR) O'zbekcha (UZ)
O'zbekcha (UZ) 中國人 (CN)
中國人 (CN)
![{\displaystyle {\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {BrCF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {Br} {}+{}\mathrm {Zn} {}\mathrel {\longrightarrow } {}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {ZnBr} {\vphantom {A}}_{\smash[{t}]{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/564bd7e448a0321b232c44d7e18f2a35605dd8a7)
![{\displaystyle {[{-}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{-}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{\vphantom {A}}^{-}]}_{n}\xrightarrow {600-700\ ^{\circ }{\text{C}},\ 130-700\ {\text{Па}}} n~{\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{=}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f02afc91cedf1a6ce9e77e87855b95f53ec19327)
![{\displaystyle {2\,\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {HCl} {}\mathrel {\longrightarrow } {}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}2\,\mathrm {HCl} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/385d1dc459990820572690cd1c625a96be441ff3)
![{\displaystyle {\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {HCl} {}\mathrel {\longrightleftharpoons } {}:\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {HCl} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d1dd0de8f7b7760c92bafcf06afc3c2e48af33ae)
![{\displaystyle {\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {HCl} {}\mathrel {\longrightleftharpoons } {}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}:{}+{}\mathrm {HCl} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d6bca9c28c601718936a187dae623e6c3be7c1f6)
![{\displaystyle {\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {HCF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {H} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/379e0e61d6d9edc5d7df3564f347d3354773ccce)
![{\displaystyle {\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{4}}{}+{}\mathrm {CO} {\vphantom {A}}_{\smash[{t}]{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/37eeec4f8592d282b903bc66090657fa2ffdc07d)
![{\displaystyle {2\,\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{=}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}\mathrm {C} {\vphantom {A}}_{\smash[{t}]{4}}\mathrm {F} {\vphantom {A}}_{\smash[{t}]{8}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/994706f646e286cf60ab012569fe806a99569447)
![{\displaystyle {\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}{\text{:}}{}\mathrel {\longrightleftharpoons } {}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{3}}{-}\mathrm {CF} {=}\mathrm {CF} {\vphantom {A}}_{\smash[{t}]{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7eac20e87935dd5c450441da5148e6e42b922cc1)